Количество теплоты. удельная теплоемкость вещества
Содержание:
- Теплопередача
- Как рассчитать количество теплоты для нагревания тела
- Шаги
- О терминах «теплота», «количество теплоты», «тепловая энергия»
- Задачи на количество теплоты с решениями
- Теплопоступления от технологического оборудования cтоловой.
- Внутренняя энергия
- Определение
- Эффективность нагревателей
- Как рассчитать количество теплоты для нагревания тела
- Термодинамика
- «Количество теплоты. Удельная теплоёмкость»
- Стремимся к тепловому равновесию: нулевое начало термодинамики
- Теплотворная способность различных видов топлива. Сравнительный анализ
Теплопередача
Теплопередача – процесс изменения внутренней энергии тела без совершения работы.
Существуют три вида теплопередачи: теплопроводность, конвекция и излучение (лучистый теплообмен). Теплопередача происходит между телами, имеющими разную температуру. Тепло передается от тела с более высокой температурой к телу с более низкой температурой.
Теплопроводность – это процесс переноса энергии от более нагретых тел (частей тела) к менее нагретым в результате движения и взаимодействия частиц тела. Высокую теплопроводность имеют металлы – так, лучшие проводники тепла – медь, золото, серебро. Теплопроводность жидкостей меньше, а газы являются плохими проводниками тепла. Пористые тела плохо проводят тепло, так как в порах содержится воздух. Вещества с низкой теплопроводностью используют в качестве теплоизоляторов. Теплопроводность невозможна в вакууме. При теплопроводности не происходит переноса вещества.
Явление теплопроводности газов аналогично явлению диффузии. Быстрые молекулы из слоя с более высокой температурой перемещаются в более холодный слой, а молекулы из холодного слоя перемещаются в более нагретый. За счет этого средняя кинетическая энергия молекул более теплого слоя уменьшается, и его температура становится ниже.
В жидкостях и твердых телах при повышении температуры какого-либо участка твердого тела или жидкости его частицы начинают колебаться сильнее. Соударяясь с соседними частицами, где температура ниже, эти частицы передают им часть своей энергии, и температура этого участка возрастает.
Конвекция – перенос энергии потоками жидкости или газа.
Объяснить механизм конвекции можно на основе теплового расширения тел и закона Архимеда. При нагревании объем жидкости увеличивается, а плотность уменьшается. Нагретый слой под действием силы Архимеда поднимается вверх, а холодный опускается вниз. Это естественная конвекция. Она возникает при неравномерном нагревании жидкости или газа снизу в поле тяготения.
При вынужденной конвекции перемещение вещества происходит под действием насосов, лопастей вентилятора. Такая конвекция применяется в состоянии невесомости. Интенсивность конвекции зависит от разности температур слоев среды и агрегатного состояния вещества. Конвекционные потоки поднимаются вверх. При конвекции происходит перенос вещества.
В твердых телах конвекция невозможна, так как частицы не могут из-за сильного взаимодействия покидать свои места. В вакууме конвекция также невозможна.
Примером конвективных потоков в природе являются ветры (бризы дневной и ночной, муссоны).
Излучение (лучистый теплообмен) – перенос энергии электромагнитными волнами. Перенос тепла излучением возможен в вакууме. Источником излучения является любое тело, температура которого отлична от нуля К. При поглощении энергия теплового излучения переходит во внутреннюю энергию. Темные тела быстрее нагреваются излучением, чем тела с блестящей поверхностью, но и остывают быстрее. Мощность излучения зависит от температуры тела. С увеличением температуры тела энергия излучения увеличивается. Чем больше площадь поверхности тела, тем интенсивнее излучение.
Как рассчитать количество теплоты для нагревания тела
Например, необходимо рассчитать количество теплоты, которое нужно потратить для того, чтобы нагреть 3 кг воды с температуры 15 0С до температуры 85 0С. Нам известна удельная теплоемкость воды, то есть количество энергии, которое нужно для того, чтобы нагреть 1 кг воды на 1 градус. То есть для того, чтобы узнать количество теплоты в нашем случае, нужно умножить удельную теплоемкость воды на 3 и на то количество градусов, на которое нужно увеличить температуры воды. Итак, это 4200*3*(85-15) = 882 000.
В скобках мы рассчитываем точное количество градусов, отнимая от конечного необходимого результата начальное
Итак, для того, чтобы нагреть 3 кг воды с 15 до 85 0С, нам потребуется 882 000 Дж количества теплоты.
Количество теплоты обозначается буквой Q, формула для его расчета выглядит следующим образом:
Q=c*m*(t2-t1).
Шаги
Часть 1 из 2:
Освойте основы
1
Ознакомьтесь с величинами, которые используются для расчета удельной теплоемкости
Очень важно знать величины, которые используются для расчета удельной теплоемкости. Вы должны знать, как выглядит символ каждой величины, и понимать, что он означает
Далее приведены величины, которые обычно используются в выражении для расчета удельной теплоемкости вещества:
Дельта, или символ «Δ», подразумевает изменение величины.
Масса образца обозначается буквой «m».
Количество теплоты обозначается буквой «Q». Единица измерения количества теплоты — «Дж», или Джоуль.
«T» — это температура вещества.
Удельная теплоемкость обозначается буквой «Cp».
2
Освойте выражение для определения удельной теплоемкости. Ознакомившись с величинами, которые используются для вычисления удельной теплоемкости, вы должны выучить уравнение для определения удельной теплоемкости вещества. Формула имеет вид: Cp = Q/mΔT.
Вы можете оперировать этой формулой, если хотите узнать изменение количества теплоты вместо удельной теплоемкости. Вот как это будет выглядеть:
Часть 2 из 2:
Вычислите удельную теплоемкость
-
1
Изучите формулу. Сначала вам нужно изучить выражение для того, чтобы понять, что вам нужно сделать, чтобы найти удельную теплоемкость. Давайте рассмотрим следующую задачу: Определите удельную теплоемкость 350 г неизвестного вещества, если при сообщении ему 34 700 дж теплоты его температура поднялась с 22 до 173 ºC без фазовых переходов.
-
2
Запишите известные и неизвестные факторы. Разобравшись с задачей, вы можете записать все известные и неизвестные переменные, чтобы лучше понять, с чем вы имеете дело. Вот как это делается:
- m = 350 г
- Q = 34 700 Дж
- ΔT = 173 ºC — 22 ºC = 151 ºC
- Cp = неизвестно
-
3
Подставьте неизвестные факторы в уравнение. Известны все значения за исключением «Cpc», поэтому необходимо подставить в исходное уравнение все остальные факторы и найти «Cp». Делать это нужно так:
- Исходное уравнение: Cp = Q/mΔT
- c = 34 700 Дж/(350 г x 151 ºC)
-
4
Найдите ответ. Теперь, после того как вы подставили известные величины в выражение, вам осталось выполнить несколько простейших арифметических действий, чтобы узнать ответ. Удельная теплоемкость — окончательный ответ — составляет 0,65657521286 Дж/(г x ºC).
- Cp = 34,700 Дж/(350 г x 151 ºC)
- Cp = 34,700 Дж/(52850 г x ºC)
- Cp = 0,65657521286 Дж/(г x ºC)
- Металл нагревается быстрее воды из-за низкой удельной теплоемкости.
- При нахождении удельной теплоемкости сокращайте единицы измерения тогда, когда это возможно.
- Удельную теплоемкость многих материалов можно найти в интернете для проверки вашего ответа.
- Иногда для изучения процессе теплопередачи в процессе физических или химических превращений может использоваться калориметр.
- Изменение температуры при прочих равных условиях значительнее для материалов с низкой удельной теплоемкостью.
- Системная единица СИ (Международная система единиц измерения) удельной теплоемкости — джоуль на градус Цельсия на грамм. В странах с британской системой мер она измеряется в калориях на градус Фаренгейта на фунт.
- Изучите формулу расчета удельной теплоемкости пищевых продуктов Cp = 4,180 x w + 1,711 x p + 1,928 x f + 1,547 x c + 0,908 x a — это уравнение для нахождения удельной теплоемкости, где «w» — процентное содержание воды в продукте, «p» — процентное содержание белков, «f» — процентное содержание жиров, «c» — процентное содержание углеводов и «a» — процентное содержание неорганических компонентов. Уравнение учитывает массовую долю (x) всех твердых веществ, которые составляют пищу. Расчет удельной теплоемкости приведен в кДж/(кг х K).
О терминах «теплота», «количество теплоты», «тепловая энергия»
Многие понятия термодинамики возникли в связи с устаревшей теорией теплорода, которая сошла со сцены после выяснения молекулярно-кинетических основ термодинамики. С тех пор они используются и в научном, и в повседневном языке. Хотя в строгом смысле теплота представляет собой один из способов передачи энергии, и физический смысл имеет лишь количество энергии, переданное системе, слово «тепло-» входит в такие устоявшиеся научные понятия, как поток тепла, теплоёмкость, теплота фазового перехода, теплота химической реакции, теплопроводность и пр. Поэтому там, где такое словоупотребление не вводит в заблуждение, понятия «теплота» и «количество теплоты» синонимичны. Однако этими терминами можно пользоваться только при условии, что им дано точное определение, не связанное с представлениями теории теплорода, и ни в коем случае «количество теплоты» нельзя относить к числу первоначальных понятий, не требующих определения. Поэтому некоторые авторы уточняют, что во избежание ошибок теории теплорода под понятием «теплота» следует понимать именно способ передачи энергии, а количество переданной этим способом энергии обозначают понятием «количество теплоты». Рекомендуется избегать такого термина, как «тепловая энергия», который по смыслу совпадает с внутренней энергией.
Задачи на количество теплоты с решениями
Формулы, используемые на уроках «Задачи на количество теплоты,
удельную теплоемкость».
1 г = 0,001 кг; 1 т = 1000 кг; 1 кДж = 1000 Дж; 1 МДж = 1000000 Дж
ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ
Задача № 1.
В железный котёл массой 5 кг налита вода массой 10 кг. Какое количество теплоты нужно передать котлу с водой для изменения их температуры от 10 до 100 °С?
При решении задачи нужно учесть, что оба тела — и котёл, и вода — будут нагреваться вместе. Между ними происходит теплообмен. Их температуры можно считать одинаковыми, т. е. температура котла и воды изменяется на 100 °С — 10 °С = 90 °С. Но количества теплоты, полученные котлом и водой, не будут одинаковыми. Ведь их массы и удельные теплоёмкости различны.

Задача № 2.
Смешали воду массой 0,8 кг, имеющую температуру 25 °С, и воду при температуре 100 °С массой 0,2 кг. Температуру полученной смеси измерили, и она оказалась равной 40 °С. Вычислите, какое количество теплоты отдала горячая вода при остывании и получила холодная вода при нагревании. Сравните эти количества теплоты.

Задача № 3.
Стальная деталь массой 3 кг нагрелась от 25 до 45 °С. Какое количество теплоты было израсходовано?

Задача № 4.
В сосуде содержится 3 л воды при температуре 20 °С. Сколько воды при температуре 45 °С надо добавить в сосуд, чтобы в нём установилась температура 30 °С? Необходимый свободный объём в сосуде имеется. Теплообменом с окружающей средой пренебречь

Задача № 5.
На сколько градусов изменилась температура чугунной детали массой 12 кг, если при остывании она отдала 648000 Дж теплоты?

Задача № 6.
По графику определите удельную теплоёмкость образца, если его масса 50 г.
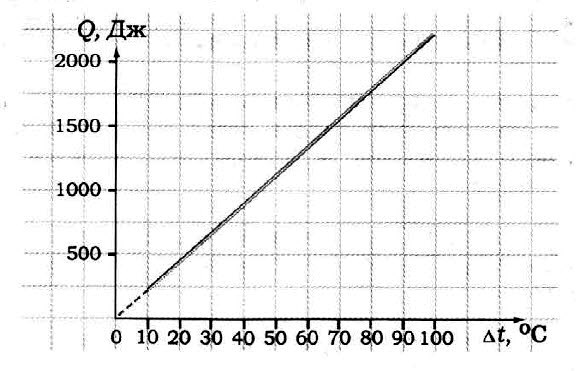

Задача № 7.
Для нагревания медного бруска массой 3 кг от 20 до 30 °С потребовалось 12000 Дж теплоты. Какова удельная теплоемкость меди?

Задача № 8.
Нагретый камень массой 5 кг, охлаждаясь в воде на 1 °С, передает ей 2,1 кДж энергии. Чему равна удельная теплоемкость камня?

Задача № 9.
Какое количество теплоты потребуется для нагревания на 1 °С воды объемом 0,5 л; олова массой 500 г; серебра объемом 2 см3; стали объемом 0,5 м3; латуни массой 0,2 т?

Задача № 10.
Какое количество теплоты получили алюминиевая кастрюля массой 200 г и находящаяся в ней вода объемом 1,5 л при нагревании от 20 °С до кипения при температуре 100 °С?

Задача № 11.
а) Воздух, заполняющий объем 0,5 л в цилиндре с легким поршнем, нагрели от 0 до 30 °С при постоянном атмосферном давлении. Какое количество теплоты получил воздух? б) В порожнем закрытом металлическом баке вместимостью 60 м3 под действием солнечного излучения воздух нагрелся от 0 до 20 °С. Как и на сколько изменилась внутренняя энергия воздуха в баке? (Удельная теплоемкость воздуха при постоянном объеме равна 720 Дж/кг-°С.)

Задача № 12.
ОГЭ
Металлический цилиндр массой m = 60 г нагрели в кипятке до температуры t = 100 °С и опустили в воду, масса которой mв = 300 г, а температура tв = 24 °С. Температура воды и цилиндра стала равной Θ = 27 °С. Найти удельную теплоёмкость металла, из которого изготовлен цилиндр. Удельная теплоёмкость воды св = 4200 Дж/(кг К).


Конспект урока «Задачи на количество теплоты».
Посмотреть конспект урока по теме «Количество теплоты. Удельная теплоемкость»
Следующая тема: «ЗАДАЧИ на сгорание топлива с решениями».
Теплопоступления от технологического оборудования cтоловой.
где: КО — коэффициент одновременности работы теплового оборудования;
для столовых КО — 0,8
для ресторанов и кафе КО — 0,7NМ — мощность установленного модулированного технологического оборудования, кВт.
Характеристика теплового оборудования предприятия общественного питания.
| Тепловое оборудование | Габариты оборудования | Установочная мощность единицы оборудования, кВт | Коэффициент загрузки оборудования КЗ |
|---|---|---|---|
| Секционное модулированное оборудование | |||
| Плиты: ПЭСМ — 4ш | 840 x 840 x 860 | 18 | 0,65 |
| ПЭСМ — 2к | 420 x 840 x 860 | 3,8 | 0,65 |
| Сковороды: | |||
| СЭСМ — 0.5 | 1470 x 840 x 860 | 13 | 0,65 |
| СЭСМ — 0.2 | |||
| Фритюрница ФЭСМ — 2 | |||
| Котел КПЭСМ — 2 | 420 x 840 x 860 | 7,5 | 0,65 |
| Шкаф ШЖЭСМ — 2 | 1050 x 840 x 860 840 x 800 x 1500 |
8,6 3,8 |
0,30 0,65 |
NН — установленная электрическая мощность не модулированного технологического оборудования, кВт;
| Тепловое оборудование | Габариты оборудования | Установочная мощность единицы оборудования, кВт | Коэффициент загрузки оборудования КЗ |
|---|---|---|---|
| Не модулированное оборудования | |||
| Варочный котел емкость, л: | |||
| 40 | — | 5 | 0,3 |
| 60 | 6,8 | 0,3 | |
| 125 | — | 8,5 | 0,3 |
| Кипятильник емкость, л: | |||
| 200 | — | 10 | 0,3 |
| 100 | — | 8,3 | 0,3 |
| 25 | — | 3,3 | 0,3 |
NР — установочная мощность электрического оборудования в раздаточном проеме, кВт;
| Тепловое оборудование | Габариты оборудования | Установочная мощность единицы оборудования, кВт | Коэффициент загрузки оборудования КЗ |
|---|---|---|---|
| Оборудование, расположенное в раздаточном проеме | |||
| Тепловая стойка СРТЭСМ | 1470 x 840 x 860 | 2,0 | 0,50 |
| Мармит МЭСМ-50 | 840 x 840 x 860 | 4,0 | 0,50 |
КЗ — коэффициент загрузки оборудования (см. таблицу);К1 — коэффициент эффективности приточно-вытяжных локализирующих устройств для модулированного оборудования — 0,75;К2 — коэффициент эффективности локализирующих устройств для немодулированного оборудования:
для приточно-вытяжных локализирующих устройств — 0,75;
для завес — 0,45.
Внутренняя энергия
Внутренняя энергия — довольно сложный термин, в смысле которого стоит разобраться прежде, чем говорить о количестве теплоты. Он обозначает ту энергию, которая изменяется при увеличении или уменьшении значения макропараметров объекта и не зависит от системы отсчета. Является частью общей энергии. Совпадает с ней в условиях, когда центр масс исследуемой вещи покоится (то есть отсутствует кинетическая составляющая).
Когда человек чувствует, что некоторый объект (скажем, велосипед) нагрелся или охладился, это показывает, что все молекулы и атомы, составляющие данную систему, испытали изменение внутренней энергии. Однако неизменность температуры не означает сохранение этого показателя.
Определение
Количество теплоты входит в математическую формулировку первого начала термодинамики, которую можно записать как Q=ΔU+A{\displaystyle Q=\Delta U+A}. Здесь Q{\displaystyle Q} — количество теплоты, переданное системе, ΔU{\displaystyle \Delta U} — изменение внутренней энергии системы и A{\displaystyle A} — работа, совершённая системой. Однако корректное определение теплоты должно указывать способ её экспериментального измерения безотносительно к первому началу. Так как теплота — это энергия, переданная в ходе теплообмена, для измерения количества теплоты необходимо пробное калориметрическое тело. По изменению внутренней энергии пробного тела можно судить о количестве теплоты, переданном от системы пробному телу, и тем самым экспериментально проверить справедливость первого начала, независимо измерив все три входящие в него величины: работу, внутреннюю энергию и теплоту. Если в феноменологической термодинамике не указать способ независимого измерения количества теплоты посредством калориметрического тела, то первое начало теряет смысл содержательного физического закона и превращается в тавтологическое определение количества теплоты.
Такое измерение можно осуществить следующим способом. Пусть в системе, состоящей из двух тел X{\displaystyle X} и Y{\displaystyle Y} и заключённой в адиабатическую оболочку, тело Y{\displaystyle Y} (пробное) отделено от тела X{\displaystyle X} жёсткой, но теплопроводящей оболочкой. Тогда оно не способно совершать макроскопическую работу, но может обмениваться энергией посредством теплообмена с телом X{\displaystyle X}. Предположим, что тело X{\displaystyle X} может совершать механическую работу, но, так как вся система адиабатически изолирована, оно может обмениваться теплотой может лишь с телом Y{\displaystyle Y}. Количеством теплоты, переданным телу X{\displaystyle X} в некотором процессе, называется величина QX=−ΔUY{\displaystyle Q_{X}=-\Delta U_{Y}}, где ΔUY{\displaystyle \Delta U_{Y}} — изменение внутренней энергии тела Y{\displaystyle Y}. Согласно закону сохранения энергии, полная работа, выполненная системой, равна убыли полной внутренней энергии системы двух тел: A=−ΔUx−ΔUy{\displaystyle A=-\Delta U_{x}-\Delta U_{y}}, где A{\displaystyle A} — макроскопическая работа, совершенная телом X{\displaystyle X}, что позволяет записать это соотношение в виде выражения для первого начала термодинамики: Q=A+ΔUx{\displaystyle Q=A+\Delta U_{x}}.
| Виды энергии: | ||
|---|---|---|
| Механическая | Потенциальная Кинетическая | |
| ‹› | Внутренняя | |
| Электромагнитная | Электрическая Магнитная | |
| Химическая | ||
| Ядерная | ||
| G{\displaystyle G} | Гравитационная | |
| ∅{\displaystyle \emptyset } | Вакуума | |
| Гипотетические: | ||
| Тёмная | ||
| См.также:Закон сохранения энергии |
Таким образом, вводимое в феноменологической термодинамике количество теплоты может быть измерено посредством калориметрического тела (об изменении внутренней энергии которого можно судить по показанию соответствующего макроскопического прибора). Из первого начала термодинамики следует корректность введённого определения количества теплоты, то есть независимость соответствующей величины от выбора пробного тела Y{\displaystyle Y} и способа теплообмена между телами. При таком определении количества теплоты первое начало становится содержательным законом, допускающим непосредственную экспериментальную проверку, кроме того, из него можно получить множество следствий, которые также проверяются в эксперименте.
Эффективность нагревателей
Мощность — это физическое определение скорости передачи или потребления энергии. Она равна отношению количества работы за определённый промежуток времени к этому периоду. Нагревательные устройства характеризуются по расходу электричества в киловаттах.
Для сопоставления энергий различного рода введена формула тепловой мощности: N = Q / Δ t, где:
- Q — количество теплоты в джоулях;
- Δ t — интервал времени выделения энергии в секундах;
- размерность полученной величины Дж / с = Вт.
В этом видео вы узнаете, как рассчитать количество теплоты:
Для оценки эффективности работы нагревателей используют коэффициент, указывающий на количество израсходованного по назначению тепла — КПД. Определяется показатель делением полезной энергии на затраченную, является безразмерной единицей и выражается в процентах. По отношению к разным частям, составляющим окружающую среду, КПД нагревателя имеет неравные значения. Если оценивать чайник как нагреватель воды, его эффективность составит 90%, а при использовании его в качестве отопителя комнаты коэффициент возрастает до 99%.
Объяснение этому простое: из-за теплообмена с окружением часть температуры рассеивается и теряется. Количество утраченной энергии зависит от проводимости материалов и других факторов. Можно рассчитать теоретически мощность тепловых потерь по формуле P = λ × S Δ T / h. Здесь λ – коэффициент теплопроводности, Вт/(м × К); S — площадь участка теплообмена, м²; Δ T — перепад температур на контролируемой поверхности, град. С; h — толщина изолирующего слоя, м.
Как рассчитать количество теплоты для нагревания тела
Например, необходимо рассчитать количество теплоты, которое нужно потратить для того, чтобы нагреть 3 кг воды с температуры 15 С до температуры 85 С. Нам известна удельная теплоемкость воды, то есть количество энергии, которое нужно для того, чтобы нагреть 1 кг воды на 1 градус. То есть для того, чтобы узнать количество теплоты в нашем случае, нужно умножить удельную теплоемкость воды на 3 и на то количество градусов, на которое нужно увеличить температуры воды. Итак, это 4200*3*(85-15) = 882 000.
В скобках мы рассчитываем точное количество градусов, отнимая от конечного необходимого результата начальное
Итак, для того, чтобы нагреть 3 кг воды с 15 до 85 С, нам потребуется 882 000 Дж количества теплоты.
Количество теплоты обозначается буквой Q, формула для его расчета выглядит следующим образом:
Q=c*m*(t2-t1).
Разбор и решение задач
Задача 1. Какое количество теплоты потребуется для нагрева 0,5 кг воды с 20 до 50 С
Дано:
m = 0,5 кг.,
с = 4200 Дж/кг*С,
t1 = 20 С,
t2 = 50 С.
Величину удельной теплоемкость мы определили из таблицы.
Решение:
количество теплоты определяется по формуле Q=c*m*(t2-t1).
Подставляем значения:
Q=4200*0,5*(50-20) = 63 000 Дж = 63 кДж.
Ответ: Q=63 кДж.
Задача 2. Какое количество теплоты потребуется для нагревания алюминиевого бруска массой 0,5 кг на 85 С?
Дано:
m = 0,5 кг.,
с = 920 Дж/кг*С,
t1 = 0 С,
t2 = 85 С.
Решение:
количество теплоты определяется по формуле Q=c*m*(t2-t1).
Подставляем значения:
Q=920*0,5*(85-0) = 39 100 Дж = 39,1 кДж.
Ответ: Q= 39,1 кДж.
Термодинамика
Рассматривать количество теплоты в отрыве от простейших процессов, на которые опирается закон сохранения энергии, не стоит – ничего не будет понятно. Поэтому для начала напомним их читателям.
Термодинамика рассматривает любую вещь или объект как соединение очень большого количества элементарных частей – атомов, ионов, молекул. Ее уравнения описывают любое изменение коллективного состояния системы как целого и как части целого при изменении макропараметров. Под последними понимаются температура (обозначается как Т), давление (Р), концентрация компонентов (как правило, С).
«Количество теплоты. Удельная теплоёмкость»
Количество теплоты
Изменение внутренней энергии путём совершения работы характеризуется величиной работы, т.е. работа является мерой изменения внутренней энергии в данном процессе. Изменение внутренней энергии тела при теплопередаче характеризуется величиной, называемой количествоv теплоты.
Количество теплоты – это изменение внутренней энергии тела в процессе теплопередачи без совершения работы. Количество теплоты обозначают буквой Q.
Работа, внутренняя энергия и количество теплоты измеряются в одних и тех же единицах — джоулях (Дж), как и всякий вид энергии.
В тепловых измерениях в качестве единицы количества теплоты раньше использовалась особая единица энергии — калория (кал), равная количеству теплоты, необходимому для нагревания 1 грамма воды на 1 градус Цельсия (точнее, от 19,5 до 20,5 °С). Данную единицу, в частности, используют в настоящее время при расчетах потребления тепла (тепловой энергии) в многоквартирных домах. Опытным путем установлен механический эквивалент теплоты — соотношение между калорией и джоулем: 1 кал = 4,2 Дж.
При передаче телу некоторого количества теплоты без совершения работы его внутренняя энергия увеличивается, если тело отдаёт какое-то количество теплоты, то его внутренняя энергия уменьшается.
Если в два одинаковых сосуда налить в один 100 г воды, а в другой 400 г при одной и той же температуре и поставить их на одинаковые горелки, то раньше закипит вода в первом сосуде. Таким образом, чем больше масса тела, тем большее количество тепла требуется ему для нагревания. То же самое и с охлаждением.
Количество теплоты, необходимое для нагревания тела зависит еще и от рода вещества, из которого это тело сделано. Эта зависимость количества теплоты, необходимого для нагревания тела, от рода вещества характеризуется физической величиной, называемой удельной теплоёмкостью вещества.
Удельная теплоёмкость
Удельная теплоёмкость – это физическая величина, равная количеству теплоты, которое необходимо сообщить 1 кг вещества для нагревания его на 1 °С (или на 1 К). Такое же количество теплоты 1 кг вещества отдаёт при охлаждении на 1 °С.
Удельная теплоёмкость обозначается буквой с. Единицей удельной теплоёмкости является 1 Дж/кг °С или 1 Дж/кг °К.
Значения удельной теплоёмкости веществ определяют экспериментально. Жидкости имеют большую удельную теплоёмкость, чем металлы; самую большую удельную теплоёмкость имеет вода, очень маленькую удельную теплоёмкость имеет золото.
Поскольку кол-во теплоты равно изменению внутренней энергии тела, то можно сказать, что удельная теплоёмкость показывает, на сколько изменяется внутренняя энергия 1 кг вещества при изменении его температуры на 1 °С. В частности, внутренняя энергия 1 кг свинца при его нагревании на 1 °С увеличивается на 140 Дж, а при охлаждении уменьшается на 140 Дж.
Количество теплоты Q, необходимое для нагревания тела массой m от температуры t1°С до температуры t2°С, равно произведению удельной теплоёмкости вещества, массы тела и разности конечной и начальной температур, т.е.
Q = c ∙ m (t2 — t1)
По этой же формуле вычисляется и количество теплоты, которое тело отдаёт при охлаждении. Только в этом случае от начальной температуры следует отнять конечную, т.е. от большего значения температуры отнять меньшее.
Это конспект по теме «Количество теплоты. Удельная теплоёмкость». Выберите дальнейшие действия:
- Перейти к следующему конспекту: «Уравнение теплового баланса»
- Вернуться к списку конспектов по Физике
- Посмотреть решение типовых задач на количество теплоты
Стремимся к тепловому равновесию: нулевое начало термодинамики
Основные законы термодинамики начинаются с нулевого начала. Возможно, эта нумерация покажется странной, ведь мало какой набор вещей из повседневной жизни начинается подобным образом (“Будь осторожен на нулевой ступеньке…”), но, знаете ли, физикам нравятся их традиции. Так вот, нулевое начало термодинамики гласит, что два тела находятся в тепловом равновесии, если они могут передавать друг другу теплоту, но не делают этого. (В русскоязычной научной литературе нулевое начало термодинамики называют также общим началом термодинамики. — Примеч. ред.)
Например, если у вас и у воды в плавательном бассейне, в котором вы находитесь, одна и та же температура, то никакое тепло от вас к воде или от воды к вам не передается (хотя такая передача возможна). Ваше тело и бассейн находятся в тепловом равновесии. Однако, если вы прыгнете в бассейн зимой, проломив при этом его ледяную корку, то первое время вряд ли будете в тепловом равновесии с его водой. Впрочем, вы и не захотите этого. (Не пытайтесь проделать этот физический опыт дома!)
Использование термометра показывает: два тела, находящиеся в тепловом равновесии с третьим, также находятся в тепловом равновесии друг с другом; вот вам еще одна формулировка нулевого начала.
Теплотворная способность различных видов топлива. Сравнительный анализ

(рис. 14.1 – Теплотворная способность топлива)
Обратите внимание на теплотворную способность (удельную теплоту сгорания) различных видов топлива, сравните показатели. Теплотворная способность топлива характеризует количество теплоты, выделяемое при полном сгорании топлива массой 1 кг или объёмом 1 м³ (1 л)
Наиболее часто теплотворная способность измеряется в Дж/кг (Дж/м³; Дж/л). Чем выше удельная теплота сгорания топлива, тем меньше его расход. Поэтому теплотворная способность является одной из наиболее значимых характеристик топлива.
Удельная теплота сгорания каждого вида топлива зависит:
- От его горючих составляющих (углерода, водорода, летучей горючей серы и др.).
- От его влажности и зольности.
| Таблица 4 – Удельная теплота сгорания различных энергоносителей, сравнительный анализ расходов. | |||||||||
| Вид энергоносителя | Теплотворная способность | Объёмнаяплотность вещества(ρ=m/V) | Цена за единицуусловного топлива | Коэфф.полезного действия (КПД) системыотопления, % | Цена за1 кВт·ч | Реализуемые системы | |||
| МДж | кВт·ч | ||||||||
| (1Мдж=0.278кВт·ч) | |||||||||
| Электричество | – | 1,0 кВт·ч | – | 3,70р. за кВт·ч | 98% | 3,78р. | Отопление, горячее водоснабжение (ГВС), кондиционирование, приготовление пищи | ||
| Метан(CH4, температуракипения: -161,6 °C) | 39,8 МДж/м³ | 11,1 кВт·ч/м³ | 0,72 кг/м³ | 5,20р. за м³ | 94% | 0,50р. | Отопление, горячее водоснабжение (ГВС), приготовления пищи, резервное и постоянное электроснабжение, автономный септик (канализация), уличные инфракрасные обогреватели, уличные барбекю, камины, бани, дизайнерское освещение | ||
| Пропан(C3H8, температуракипения: -42.1 °C) | 46,34МДж/кг | 23,63МДж/л | 12,88кВт·ч/кг | 6,57кВт·ч/л | 0,51 кг/л | 18,00р. за л | 94% | 2,91р. | Отопление, горячее водоснабжение (ГВС), приготовления пищи, резервное и постоянное электроснабжение, автономный септик (канализация), уличные инфракрасные обогреватели, уличные барбекю, камины, бани, дизайнерское освещение |
| БутанC4H10, температуракипения: -0,5 °C) | 47,20МДж/кг | 27,38МДж/л | 13,12кВт·ч/кг | 7,61кВт·ч/л | 0,58 кг/л | 14,00р. за л | 94% | 1,96р. | Отопление, горячее водоснабжение (ГВС), приготовления пищи, резервное и постоянное электроснабжение, автономный септик (канализация), уличные инфракрасные обогреватели, уличные барбекю, камины, бани, дизайнерское освещение |
| Пропан-бутан(СУГ – сжиженный углеводородный газ) | 46,8МДж/кг | 25,3МДж/л | 13,0кВт·ч/кг | 7,0кВт·ч/л | 0,54 кг/л | 16,00р. за л | 94% | 2,42р. | Отопление, горячее водоснабжение (ГВС), приготовления пищи, резервное и постоянное электроснабжение, автономный септик (канализация), уличные инфракрасные обогреватели, уличные барбекю, камины, бани, дизайнерское освещение |
| Дизельное топливо | 42,7МДж/кг | 11,9кВт·ч/кг | 0,85 кг/л | 30,00р. за кг | 92% | 2,75р. | Отопление (нагрев воды и выработка электричества – очень затратны) | ||
| Дрова(берёзовые, влажность – 12%) | 15,0МДж/кг | 4,2кВт·ч/кг | 0,47-0,72 кг/дм³ | 3,00р. за кг | 90% | 0,80р. | Отопление (неудобно готовить пищу, практически невозможно получать горячую воду) | ||
| Каменный уголь | 22,0МДж/кг | 6,1кВт·ч/кг | 1200-1500 кг/м³ | 7,70р. за кг | 90% | 1,40р. | Отопление | ||
| МАРР газ (смесь сжиженного нефтяного газа – 56% с метилацетилен-пропадиеном – 44%) | 89,6МДж/кг | 24,9кВт·ч/м³ | 0,1137 кг/дм³ | -р. за м³ | 0% | Отопление, горячее водоснабжение (ГВС), приготовления пищи, резервное и постоянное электроснабжение, автономный септик (канализация), уличные инфракрасные обогреватели, уличные барбекю, камины, бани, дизайнерское освещение |
(рис. 14.2 – Удельная теплота сгорания)
Согласно таблице «Удельная теплота сгорания различных энергоносителей, сравнительный анализ расходов», пропан-бутан (сжиженный углеводородный газ) уступает в экономической выгоде и перспективности использования только природному газу (метану).
Однако следует обратить внимание на тенденцию к неизбежному росту стоимости магистрального газа, которая на сегодняшний день существенно занижена. Аналитики предрекают неминуемую реорганизацию отрасли, которая приведёт к существенному удорожанию природного газа, возможно, даже превысит стоимость дизельного топлива
Таким образом, сжиженный углеводородный газ, стоимость которого практически не изменится, остаётся исключительно перспективным – оптимальным решением для систем автономной газификации.