Удельная теплота сгорания
Содержание:
- Характеристика керосина как топлива
- Удельная теплота сгорания жидкого топлива (спирта, бензина, керосина, нефти)
- Топливо и его горение
- Сборник задач по физике, Лукашик В.И.
- Откуда берется тепло в процессе горения?
- Температура кипения солярки
- Камера сгорания
- Дизельный двигатель
- Особенности печи, работающей на угле
- Расчет горения смеси природного и доменного газов.
- Услуги
- Оборудование
- Откуда берется энергия у топлива
- Дрова
Характеристика керосина как топлива
Горением называют процесс бурного окисления веществ с выделением тепла. Как правило, в реакции участвует кислород, содержащийся в воздухе. Во время сжигания углеводородов образуются такие основные продукты горения:
- углекислый газ;
- водяной пар;
- сажа.
Количество энергии, генерируемое во время сгорания топлива, зависит от его вида, условий сжигания, массы или объёма. Энергия измеряется в джоулях или калориях. Удельной (на единицу измерения количества вещества) теплотой сгорания называют энергию, полученную при сжигании единицы топлива:
- молярная (например, Дж/моль);
- массовая (например, Дж/кг);
- объёмная (например, ккал/л).
 Во время сжигания углевода образуется несколько элементов, например, сажа
Во время сжигания углевода образуется несколько элементов, например, сажа
Значение теплоты сгорания будет зависеть от того, брались ли в учёт процессы, происходящие с водой во время сгорания. Испарение влаги — энергоёмкий процесс, а учёт теплоотдачи при конденсации этих паров также способен повлиять на результат.
Результат замеров, производимых до того, как сконденсированный пар вернёт энергию в систему, называют низшей теплотой сгорания, а показатель, полученный после конденсации паров, называется высшей теплотой. Углеводородные двигатели не могут использовать дополнительную энергию водяного пара в выхлопе, поэтому показатель нетто актуален для производителей моторов и встречается в справочниках чаще.
Нередко при указании теплотворной способности не уточняют о том, какая из величин имеется в виду, что может привести к путанице. Сориентироваться помогает знание того, что в РФ традиционно принято указывать низшую.
 Низшая теплота сгорания – важный показатель
Низшая теплота сгорания – важный показатель
Следует отметить, что для некоторых видов топлива разделение на энергию нетто и брутто не имеет смысла, так как они не образуют воду во время горения. В отношении керосина это неактуально, поскольку содержание углеводородов в нём велико. При сравнительно невысокой плотности (между 780 кг/м³ и 810 кг/м³) его теплотворная способность аналогична этому же показателю у дизельного топлива и составляет:
- низшая — 43,1 МДж/кг;
- высшая — 46,2 МДж/кг.
Удельная теплота сгорания жидкого топлива (спирта, бензина, керосина, нефти)
Приведена таблица удельной теплоты сгорания жидкого топлива и некоторых других органических жидкостей. Следует отметить, что высоким тепловыделением при сгорании отличаются такие топлива, как: бензин, авиационный керосин, дизельное топливо и нефть.
Удельная теплота сгорания спирта и ацетона существенно ниже традиционных моторных топлив. Кроме того, относительно низким значением теплоты сгорания обладает жидкое ракетное топливо и этиленгликоль — при полном сгорании 1 кг этих углеводородов выделится количество теплоты, равное 9,2 и 13,3 МДж, соответственно.
| Топливо | Удельная теплота сгорания, МДж/кг |
|---|---|
| Ацетон | 31,4 |
| Бензин А-72 (ГОСТ 2084-67) | 44,2 |
| Бензин авиационный Б-70 (ГОСТ 1012-72) | 44,1 |
| Бензин АИ-93 (ГОСТ 2084-67) | 43,6 |
| Бензол | 40,6 |
| Дизельное топливо зимнее (ГОСТ 305-73) | 43,6 |
| Дизельное топливо летнее (ГОСТ 305-73) | 43,4 |
| Жидкое ракетное топливо (керосин + жидкий кислород) | 9,2 |
| Керосин авиационный | 42,9 |
| Керосин осветительный (ГОСТ 4753-68) | 43,7 |
| Ксилол | 43,2 |
| Мазут высокосернистый | 39 |
| Мазут малосернистый | 40,5 |
| Мазут низкосернистый | 41,7 |
| Мазут сернистый | 39,6 |
| Метиловый спирт (метанол) | 21,1 |
| н-Бутиловый спирт | 36,8 |
| Нефть | 43,5…46 |
| Нефть метановая | 21,5 |
| Толуол | 40,9 |
| Уайт-спирит (ГОСТ 313452) | 44 |
| Этиленгликоль | 13,3 |
| Этиловый спирт (этанол) | 30,6 |
Топливо и его горение
Основным источником энергии для металлургической промышленности является топливо.
Под топливом понимают вещество, горение которого сопровождается выделением значительного количества тепла и которое отвечает следующим требованиям:
-
запасы должны быть достаточными для того, чтобы их было экономически выгодно добывать и попользовать;
-
продукты сгорания должны легко удаляться из зоны горения;
-
продукты сгорания должны быть безвредны для окружающего мира и самих тепловых устройств;
-
процесс горения должен быть легко управляем.
Этим требованиям отвечают органические соединения, содержащие углерод С и водород Н и их соединения.
Все виды топлива подразделяют на естественное и искусственное, каждое из которых в свою очередь подразделяются на твердое, жидкое, газообразное.
Химический состав топлива.
Топливо состоят из горючей массы и балласта. К горючим компонентам относятся С, Н, S (сера органическая и колчеданная). В состав топлива входят азот N (не горит, теплоноситель), кислород О (окисляет горючие компоненты).
Кроме этого в топливе всегда присутствуют вода и зола. Вода, содержащаяся в топливе, подразделяется на гигроскопическую, химически связанную и внешнюю, которая механически удерживается в топливе и теряется при сушке.
Зола – это негорючая минеральная часть топлива, состоящая из Al2O3, Fe2O3, Si2O3, CaO и др.
Элементарный анализ топлива.
|
Индекс |
Состав |
|||||
|
C |
H |
O |
N |
S |
A |
W |
|
О |
органическая масса |
|||||
|
Г |
горючая масса |
|||||
|
С |
сухая масса |
|||||
|
Р |
рабочая масса |
Состав рабочего топлива:
СР + HР + OР + NР + SР + AР + WР = 100%
Пересчет состава топлива с любой массы на рабочее топливо выполняется по одному из следующих выражений:
Теплота сгорания топлива.
Количество выделившегося тепла при сжигании топлива связано с химическим составом топлива.
Количество тепла, которое выделяется при сжигании единицы топлива, называется теплотой сгорания топлива Q. Ее размерности: кДж/кг (ккал/кг), кДж/м3 (ккал/м3) или кДж/кмоль (ккал/кмоль).
В технике различают высшую Qв и низшую Qн теплоту сгорания топлива. Под низшей теплотой сгорания понимают то количество тепла, которое выделяется при сжигании единицы топлива до продуктов полного сжигания при условии, что вода, содержащаяся в продуктах сгорания, находится в виде пара, охлажденного до 20оС.
Теплота сгорания топлива определяется по следующим формулам:
для твердого и жидкого топлива:
для газообразного:
,
где CP, HP, CO, H2 и т.д. – составляющие топлив, %;
4, 187кДж = 1ккал.
Условное топливо.
Для удобства планирования, учета и сравнения различных видов топлива введено понятие условного топлива, которое характеризуется низшей теплотой сгорания
.
Для перевода натурального топлива в условное находится эквивалент данного топлива:
для твердого и жидкого:
для газообразного:
.
Перерасчет расхода натурального топлива Вр на условное Ву осуществляется по формуле:
Газообразное топливо.
Газообразное топливо по сравнению с твердым и жидким топливом обладает следующими преимуществами:
-
возможностью лучшего смешения газа с воздухом и, следовательно, сжиганием с меньшим избытком воздуха;
-
легкостью подогрева перед сжиганием;
-
отсутствием золы;
-
транспортабельностью и удобством учета расхода газа;
-
простотой обслуживания горелочных устройств.
Недостатки: взрывоопасность, малая объемная масса (требуются большие емкости для хранения).
Природный газ – наиболее дешевое топливо. Его основным горючим компонентом является метан CH4 = 95%.
Искусственные газы:
-
коксовый газ – продукт коксования углей;
горючие компоненты – Н2 = 46-60%; СН4 = 20-30%; МДж/м3;
-
доменный (колошниковый) газ получают в процессе доменной плавки, содержит около 30% СО; МДж/м3.
Жидкое топливо.
Естественное жидкое топливо – нефть. Как топливо ее используют редко.
Искусственное жидкое топливо – это продукты переработки нефти: бензин, лигроин, керосин, газойль и др. Остаток переработки – мазут. Мазут – топливо металлургической промышленности и энергетики. Перед сжиганием мазут нагревают до 70-80оС с целью понижения его вязкости. Состав мазута – это соединения углеродов. С = 85-88%; Н2 = 10%; МДж/кг.
Твердое топливо.
Это каменный и бурый угли, антрацит, горючие сланцы, торф.
Основной метод переработки угля – коксование, заключающийся в сухой перегонке топлива путем нагрева угля без доступа воздуха при температурах 900-1100оС в коксовых печах. Получается спекшийся кокс, пористый, механически прочный, применяемый в металлургии, в основном для выплавки чугуна. Содержание С=75-85%; МДж/кг.
Сборник задач по физике, Лукашик В.И.
1033. Какие дрова — березовые, сосновые или осиновые — при полном сгорании выделяют больше теплоты, если все они одинаково высушены и массы их равны? (Удельная теплота сгорания осины около 1,3 • 107 Дж/кг.) Удельная теплота всех этих дров одинакова, поэтому при их сгорании выделится одинаковое количество теплоты.
1034. Можно ли рассчитать, какое количество теплоты выделится при полном сгорании соснового полена? Если можно, то как это сделать, что необходимо знать? Можно. Для этого надо знать удельную теплоту сгорания и массу полена.
1035. Вычислите, сколько энергии выделится при полном сгорании древесного угля массой 15 кг; керосина массой 200 г.
1036. Какое количество теплоты выделится при полном сгорании бензина массой 5 кг; каменного угля массой 10 кг?
1037. Какое количество теплоты выделится при полном сгорании пороха массой 25 г; торфа массой 0,5 т; каменного угля массой 1,5 т?
1038. Сколько теплоты выделится при полном сгорании сухих березовых дров объемом 5 м3?
1039. Сколько теплоты выделится при полном сгорании керосина объемом 0,25 м3; спирта объемом 0,00005 м3; бензина объемом 25 л; нефти объемом 250 л?
1040. На сколько больше теплоты выделится при полном сгорании бензина массой 2 кг, чем при сгорании сухих березовых дров той же массы?
1041. Во сколько раз больше выделится теплоты при полном сгорании водорода массой 1 кг, чем при полном сгорании сухих березовых дров той же массы?
1042. Смешали бензин массой 2 кг и керосин массой 3 кг. Какое количество теплоты выделится при полном сгорании полученного топлива?
1043. Смешали бензин объемом 1,5 л и спирт объемом 0,5 л. Какое количество теплоты выделится при полном сгорании этого топлива?
1044. В печи сгорели сухие сосновые дрова объемом 0,01 м3 и торф массой 5 кг. Сколько теплоты выделилось в печи?
1045. К зиме заготовили сухие сосновые дрова объемом 2 м3 и каменный уголь массой 1,5 т. Сколько теплоты выделится в печи при полном сгорании в ней заготовленного топлива?
1046. а) При полном сгорании антрацита (твердое топливо) массой 10 кг выделяется 2,9 • 107 Дж энергии. Чему равна удельная теплота сгорания антрацита? б) В лифте высотного здания Московского университета студент поднялся со спортивным грузом (4 спортивных молота). На какую высоту был поднят груз, если его потенциальная энергия относительно пола первого этажа здания стала эквивалентна энергии, выделяемой при полном сгорании 1 г нефти? (Сведения о грузе смотри в таблице 17.)
1047. На какой высоте над поверхностью океана летела в самолете команда футболистов в то время, когда потенциальная энергия их футбольного мяча в самолете была эквивалентна количеству теплоты, которая выделяется при полном сгорании 1 г нефти? (О мяче смотри таблицу 17.)
1048. Сколько нужно сжечь каменного угля, чтобы выделилось 1,5 • 108 Дж энергии; 1,8 • 105 кДж энергии?
1049. В топке котла парового двигателя сожгли торф массой 20 т. Какой массой каменного угля можно было бы заменить сгоревший торф? (Удельную теплоту сгорания торфа принять равной 1,5 • 107 Дж/кг.)
1050. Сколько каменного угля нужно сжечь, чтобы получить столько же энергии, сколько ее выделяется при сгорании бензина объемом 6 м3?
1051. Сколько спирта надо сжечь, чтобы изменить температуру воды массой 2 кг от 14 до 50 °С, если вся теплота, выделенная при горении спирта, пойдет на нагревание воды?
1052. Сколько воды, взятой при температуре 14 °С, можно нагреть до 50 °С, сжигая спирт массой 30 г и считая, что вся выделяемая при горении спирта энергия идет на нагревание воды?
1053. На сколько изменится температура воды объемом 100 л, если считать, что вся теплота, выделяемая при сжигании древесного угля массой 0,5 кг, пойдет на нагревание воды?
1054. На сколько изменится температура воды, масса которой 22 кг, если ей передать всю энергию, выделившуюся при сгорании керосина, масса которого равна 10 г?
Откуда берется тепло в процессе горения?
Сам по себе процесс сгорания топлива — это химическая, окислительная реакция. Большинство видов топлива содержит большое количество углерода С, водорода H, серы S и других веществ. Во время горения атомы C, H, и S соединяется с атомами кислорода О2, в результате чего получается молекулы СО, СО2, Н2О, SO2. При этом происходит выделение большого количества тепловой энергии, которую люди научились использовать в своих целях.
Рис. 1. Виды топлива: уголь, торф, нефть, газ.
Основной вклад в выделение тепла дает углерод C. Второй по количеству тепла вклад вносит водород H.
Рис. 2. Атомы углерода вступают в реакцию с атомами кислорода.
Температура кипения солярки
Температура кипения солярки, как и во всех указанных выше факторах, зависит от климатических особенностей горючего. Она может варьироваться от 180 до 370 С, причем данный показатель критически важен для любых расчетов.
Кипение на практике – это процесс перехода из жидкого состояния в газообразное, в котором момент вспышки значительно изменяется. Соблюдение данного параметра производителями гарантирует, что сгорание топлива будет полным с максимальным выделением энергии, а выбросы в окружающую среду окажутся минимальными.
Горит ли дизельное топливо? Горит, причем достаточно сильно. Его остаток, который не участвовал в предварительно смешанном сгорании, расходуется в фазе сгорания с регулируемой скоростью.
Сжигание в дизельных двигателях очень сложно. До 90-х годов прошлого столетия его детальные механизмы не были хорошо поняты. Температура горения дизельного топлива в камере сгорания также варьировалась от случая к случаю. На протяжении десятилетий сложность данного процесса, казалось, не поддалась попыткам исследователей раскрыть его многочисленные секреты, несмотря на наличие современных инструментов, таких как высокоскоростная фотография, используемая в «прозрачных» двигателях, вычислительная мощность современных компьютеров и множество математических моделей, предназначенных для имитации сгорания в дизеле. Применение лазерной визуализации листа к традиционному процессу сжигания дизельного топлива в 90-х годах прошлого века стало ключом к значительному углублению понимания этого процесса.
В этой статье будет рассмотрена наиболее устоявшаяся модель процесса для классического дизельного двигателя. Это обычное сгорание дизельного топлива, в первую очередь, контролируется смешиванием, которое может происходить из-за диффузии горючего и воздуха перед воспламенением.

Камера сгорания
Ключевая цель при ее проектировании заключается в том, чтобы обеспечить достаточное смешивание топлива и воздуха для смягчения воздействия областей, богатых горючим, и позволить двигателю достичь своих показателей производительности и выбросов. Обнаружено, что турбулентность в движении воздуха внутри камеры сгорания полезна для процесса перемешивания и может быть использована для достижения этой цели. Вихрь, создаваемый впускным отверстием, может усиливаться, а поршень может создавать сдавливание, когда он приближается к головке цилиндра, чтобы обеспечить больше турбулентности во время акта сжатия благодаря правильной конструкции чаши в головке поршня.
Конструкция камеры сгорания оказывает наиболее значительное влияние на выбросы твердых частиц. Она также может влиять на несгоревшие углеводороды и СО. Хотя выбросы NOx зависят от конструкции чаши , свойства объемного газа играют очень важную роль в уровнях их выхлопных газов. Однако из-за компромисса с NOx / PM конструкции камер сгорания должны были развиваться по мере уменьшения пределов выбросов NOx. В основном это требуется, чтобы избежать увеличения выбросов PM, которые в противном случае могли бы возникнуть.
Читать также: Лицензия такси выдается на машину или человека
Дизельный двигатель
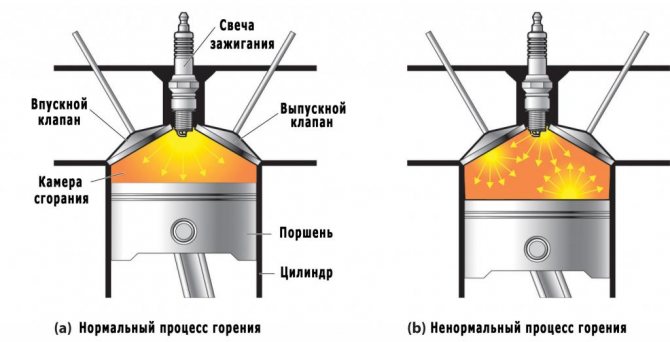
Он назван в честь изобретателя Рудольфа Дизеля. Является двигателем внутреннего сгорания, в котором воспламенение впрыскиваемого топлива вызывается повышенной температурой воздуха в цилиндре из-за механического сжатия. Дизель работает, сжимая только воздух. Это повышает температуру воздуха внутри цилиндра до такой степени, что распыленное топливо, впрыскиваемое в камеру сгорания, самовозгорается.
Это отличается от двигателей с искровым зажиганием, таких как бензиновый или газовый (использующий газообразное горючее, а не бензин). В них используют свечу зажигания для воспламенения топливовоздушной смеси. В дизельных двигателях свечи накаливания (подогреватели камеры сгорания) могут применяться для облегчения запуска в холодную погоду, а также при низкой степени сжатия. Оригинальный дизель работает по циклу постоянного давления постепенного сгорания и не производит звукового удара.
Особенности печи, работающей на угле
Подобное устройство имеет конструктивные особенности, предполагает проведение реакции пиролиза угля. Древесный уголь не относится к полезным ископаемым, он стал продуктом человеческой деятельности.
Температура горения угля составляет 900 градусов, что сопровождается выделением достаточного количества тепловой энергии. Какова технология создания такого удивительного продукта? Суть заключается в определенной обработке древесины, благодаря чему происходит существенное изменение ее структуры, выделение из нее избыточной влаги. Осуществляется подобный процесс в специальных печах. Принцип действия таких устройств базируется на процессе пиролиза. Печь для получения древесного угля состоит из четырех базовых компонентов:
- камеры сгорания;
- укрепленного основания;
- дымохода;
- отсека вторичной переработки.

Расчет горения смеси природного и доменного газов.
Исходные данные для расчета
-
Состав сухого природного и доменного газов, %
|
Газ |
CO |
CO2 |
CH4 |
C2H6 |
C3H8 |
C4H10 |
C5H12 |
H2 |
N2 |
O2 |
∑ |
|
Природный |
— |
0,5 |
85,0 |
4,0 |
2,5 |
1,5 |
1,5 |
— |
5,0 |
— |
100 |
|
Доменный |
27 |
12,7 |
0,3 |
— |
— |
— |
— |
1,4 |
58,6 |
— |
100 |
-
Коэффициент расхода воздуха: n = 1,14;
-
Содержание влаги в доменном газе: Wд.г. = 44г/м3;
-
Содержание влаги в природном газе: Wп.г. = 0г/м3 (газ сухой);
-
Теплота сгорания смеси: ;
-
Температура подогрева воздуха и газа: tВ = 600оС = 873К;
tГ = 400оС = 673К;
-
Температура уходящих продуктов сгорания (дыма): tП.Г. = 840оС = 1113К;
-
Расчет ведется на 1м3 газа.
Расчет состава природно-доменной смеси.
1. Пересчет состава сухого доменного газа на влажный.
Объемный процент водяных паров во влажном доменном газе:
.
Коэффициент пересчета состава сухого доменного газа во влажный (рабочий):
.
Рабочий состав доменного газа:
;
;
;
;
.
Таблица 1. Состав рабочего доменного газа.
|
Газ |
СН4 |
СО2 |
H2 |
CO |
N2 |
H2O |
∑ |
|
Доменный |
0,285 |
12,039 |
1,337 |
25,596 |
55,553 |
5,19 |
100 |
2. Определение теплоты сгорания газов .
Природного газа:
.
Доменного газа:
.
3. Расчет состава смеси природного и доменного газов.
Принимаем долю доменного газа в природно-доменной смеси (ПДС) за x, тогда доля природного газа будет равна y = (1-x). Составляем уравнение:
,
где – исходная теплота сгорания смеси газов, МДж/м3.
Находим, что
.
у = (1-х) = 1-0,747 = 0,253.
Состав смешанного газа, %.
;
Таблица 2. Состав природно-доменной смеси.
|
CO |
CO2 |
CH4 |
C2H6 |
C3H8 |
C4H10 |
N2 |
H2 |
H2O |
∑ |
|
20,48 |
9,1196 |
21,7877 |
1,0314 |
0,7448 |
0,4641 |
41,0975 |
1,0185 |
3,8769 |
100 |
Проверка:
Погрешность: 0,004%.
4. Плотность ПДС и воздуха.
Плотность ПДС.
.
Плотность воздуха.
5. Расход воздуха, необходимого для сжигания единицы топлива.
Теоретический расход воздуха (n = 1).
Действительный расход воздуха (n = 1,14).
6. Расчет количества и состава продуктов сгорания.
Объем углекислого газа в ПГ:
Объем водяных паров в ПГ:
Объем азота в ПГ:
Объем избыточного кислорода в ПГ:
Общее количество ПС:
Состав ПС:
Таблица 3. Состав продуктов сгорания.
|
Продукты сгорания |
СО2 |
Н2О |
N2 |
O2 |
∑ |
|
% |
13,1626 |
12,8199 |
71,9703 |
2,0472 |
100 |
Плотность ПС:
7. Материальный баланс процесса горения.
|
Приход, кг |
Расход, кг |
Невязка баланса, % |
|
1. Газ: |
Продукты сгорания: |
|
|
2. Воздух: |
||
|
Всего: 5,728кг |
5,723кг |
8. Определение калориметрической температуры горения.
Находим начальную энтальпию продуктов сгорания по формуле, где известно физическое тепло подогретого газа и воздуха.
Физическое тепло газа:
где – теплоемкость подогретого газа при t = 400oC, найденная по формуле:
где:
-
теплоемкости , и т.д., а также Св – теплоемкость подогретого воздуха берем из таблицы №4 (Расчет горения газообразного топлива. Методические указания к курсу «Теплотехника», Алматы – 1983г.);
-
теплоемкости для газов метанового ряда берем из таблицы №5 (там же).
Физическое тепло подогретого воздуха:
.
Начальная энтальпия продуктов сгорания:
.
По величине , используя таблицу №7 (там же), находим приближенное значение .
Определяем энтальпию продуктов горения при этой температуре:
Значения , и т.д. находим из таблицы №6 (там же).
Полученное значение , значит, .
Находим – энтальпию продуктов сгорания при 2000оС:
Получилось, что , т.е. действительно калориметрическая температура лежит в интервале (), которая равна:
.
Использованная литература: Расчет горения газообразного топлива. Методические указания к
курсу «Теплотехника». – Алматы.: Минвуз Казахской ССР, 1983. – 32с.
Услуги
- Оборудование
- Проектирование газораспределительных систем
- Строительно-монтажные, пуско-наладочные работы
Оборудование
- Оборудование в наличии
- Резервуары для хранения СУГ
- Газовые заправочные станции FAS
- Автономное газоснабжение частных домов и котеджей
- Автономное газоснабжение промышленных объектов
- Испарители
- Насосы и насосные агрегаты для СУГ
- Компрессора для СУГ
- Газозаправочные колонки
- Универсальные газовые колонки
- Наполняющее оборудование для бытовых баллонов
- Массовые расходомеры FAS
- Арматура для СУГ (краны, фильтры, клапаны, шланги и т.д.)
- Промышленные компрессоры CORKEN
- Промышленное насосное оборудование
- Газоснабжение теплиц
- Газонаполнительные станции (ГНС)
- Газгольдеры
- Фланцы
Откуда берется энергия у топлива
Известно, что молекулы состоят из атомов. Для того, чтобы разделить какую либо молекулу (например, молекулу воды) на составляющие её атомы, требуется затратить энергию (на преодоление сил притяжения атомов). Опыты показывают, что при соединении атомов в молекулу (это и происходит при сжигании топлива) энергия, напротив, выделяется.
Как известно, существует ещё и ядерное топливо, но мы не будем здесь говорить о нём.
При сгорании топлива выделяется энергия. Чаще всего это тепловая энергия. Опыты показывают, что количество выделившейся энергии прямо пропорционально количеству сгоревшего топлива.
Дрова
Это пиленные либо колотые куски дерева, которые во время сжигания в печах, котлах и прочих устройствах вырабатывают тепловую энергию.
Для удобства загрузки в топку древесный материал разрезают на отдельные элементы длиной до 30 см. Чтобы повысить эффективность от их использования, дрова должны быть максимально сухими, а процесс горения – относительно медленным. По многим параметрам для отопления помещений подходят дрова из таких лиственных пород, как дуб и береза, лещина и ясень, боярышник. Из-за высокого содержания смолы, повышенной скорости горения и низкой теплотворности хвойные деревья в этом плане значительно уступают.
Следует понимать, что на величину показателя теплотворности влияет плотность древесины.
| Дрова (естественная сушка) | Теплотворная способность кВт⋅ч/кг | Теплотворная способность мега Дж/кг |
| Грабовые | 4,2 | 15 |
| Буковые | 4,2 | 15 |
| Ясеневые | 4,2 | 15 |
| Дубовые | 4,2 | 15 |
| Березовые | 4,2 | 15 |
| Из лиственницы | 4,3 | 15,5 |
| Сосновые | 4,3 | 15,5 |
| Еловые | 4,3 | 15,5 |